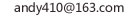与4.8gCH4含相同质子数目的SO2的质量为 ( ) g?
1L滚,占版面碍眼
因为每58.5gNaCl就是1mol,(这就是氯化钠的摩尔质量的意思)所以117g,也就是有2个58.5,那么就是2mol了。 那我们现在再看看公式:n=m/M, 现在m为117g,M为58.5g/mol,那么117/58.5就是等于2,单位为mol。所以就是2mol。
通过理解公式上的每个字母的意思,再来看公式,你就能从本质上理解,其他的那几个公式也是那样的。好好地学好这个知识吧,这很重要的。 就是这样,理解了吗?
S:16个质子,O:8个质子,SO4质子数=16*1+8*2=32
所需SO4=3/32mol
SO2的质量=3/32*32=3g
希望可以帮到你
望采纳本回答被提问者采纳
H- 1
S- 16
O- 8
CH4- 10 16
SO2- 32 64
相同质子数目的CO2与SO2质量之比 32/12*16/64=4/3
所以答案是3/4*4.8g=3.6g
高一化学!关于“物质的量”这一部分所有的概念和计算公式!要详细...
1. 物质的质量=物质的量 × 该物质的摩尔质量即 m = nM。其中摩尔质量数值等于该物质的相对分子质量或相对原子质量。2. 物质的量计算中的其他公式包括:气体体积与物质的量的关系,以及涉及化学反应方程式中的物质的量计算等。三、详细解释 物质的量:它是衡量微观粒子集合的一个物理量,比如原子、分...
高一化学摩尔公式总结是什么?
高一化学摩尔公式总结如下:1. 物质的量(n)可以通过质量(m)除以摩尔质量(M)来计算,即 n = m\/M。2. 对于气体,物质的量(n)可以通过粒子数(N)除以阿伏伽德罗常数(NA)来确定,即 n = N\/NA。3. 物质的量浓度(n)可以通过体积(V)除以摩尔体积(Vm)来得出,即 n = V\/Vm。4....
高一化学与“物质的量”有关的所有公式
在高一化学中,物质的量是一个基础且重要的概念。通常,物质的量n用以下公式表示:n=m\/M=N\/NA=V(L)\/22.4。其中,m代表物质的质量,M代表摩尔质量,N是物质中的分子或原子数目,NA是阿伏伽德罗常数,V(L)是物质的体积,22.4是标准状况下的气体摩尔体积。这个公式帮助我们通过不同的量来计算...
求高一化学物质的量的计算相关公式
在高中化学学习中,物质的量是化学计算的基础。物质的量(n)的计算涉及多个公式,最基本的是n=m\/M。这里,m代表物质的质量(单位:克),M是物质的摩尔质量(单位:克\/摩尔)。这个公式适用于任何物质,只要知道其质量及摩尔质量。另一个常用的公式是n=V\/Vm,其中V表示气体在标准状况下的体积(单...
高一刚学化学 问三个有关物质的量的小计算
2、5ml溶液的物质的量浓度与200ml溶液的物质的量浓度时相同的。根据c1v1=c2v2 5 mol\/L × 10 Ml = c2 ×200mL c2 = 0.25 mol \/ L 3、可以写出方程式:MCln + n NaOH = n NaCl + M(OH)n 由此得知:n (MCln) \/ n(NaOH) = 1\/n 0.50mol\/L ×10.00mL \/ (0...
高一化学!关于“物质的量”这一部分所有的概念和计算公式!要详细!_百度...
物质的量的单位是摩(尔),符号:mol,标准:0.012 kg 12C所含的碳原子数.在使用物质的量时,必须指明基本单元。一般利用化学式指明基本单元,而不用汉字。使用摩尔时,基本单元应指明,可以是原子分子及其粒子,或这些粒子的特定组合。2、阿伏伽德罗常数(NA)以0.012kg12C所含的碳原子数作基准,其...
高一化学!关于“物质的量”这一部分所有的概念和计算公式!要详细!_百度...
的体积大约为22.4升。此外,物质的量与其它物理量之间的关系也可以通过一些公式来表示,如n=N\/NA=m\/M=V\/Vm=cV。这些关系式可以帮助我们更好地理解和计算物质的量在不同条件下的变化。希望上述内容能够帮助你在学习高一化学时更好地掌握“物质的量”的相关概念和计算方法,祝你学习顺利!
高一化学物质的量计算公式
在高一化学的学习过程中,我们常常会接触到物质的量这一重要概念。物质的量是表示物质基本单元的数量,是国际单位制中的七个基本物理量之一。其定义为物质的粒子数除以阿伏加德罗常数,用公式表示为n=N\/NA,这里的N代表粒子数,NA为阿伏加德罗常数,通常取值为6.022×10^23 mol^-1。通过这个公式,我们...
高一化学的物质的量这个专题 计算公式
通过上述公式,可以计算出物质的质量、摩尔质量或物质的量。例如,已知m=18g,M=18g\/mol,则n=m\/M=1mol。同样,若已知n=2mol,M=35.5g\/mol,则m=nM=71g。理解这些公式和概念时,应注意每个物理量的单位,如摩尔质量的单位为g\/mol,而相对原子质量、相对分子质量或化学式的式量无单位。通过...
高一化学!关于“物质的量”这一部分所有的概念和计算公式!要详细!_百度...
在化学计算中,物质的量浓度(mol\/L)是描述溶液中溶质含量的物理量,它是单位体积溶液中溶质的物质的量。例如,1 mol\/L的NaCl溶液意味着每升溶液中含1摩尔的NaCl。理解并熟练运用物质的量、阿伏加德罗常数和摩尔质量等概念,是高一化学学习中不可或缺的基础。这些概念帮助我们量化化学反应,进行微观和...